Laboratoire Léon Brillouin
UMR12 CEA-CNRS, Bât. 563 CEA Saclay
91191 Gif sur Yvette Cedex, France
+33-169085241 llb-sec@cea.fr
Laboratoire Léon Brillouin
UMR12 CEA-CNRS, Bât. 563 CEA Saclay
91191 Gif sur Yvette Cedex, France
+33-169085241 llb-sec@cea.fr


|
Des solutions savonneuses qui moussent, cela n’est pas extraordinaire ; une mousse de savon stable pendant plusieurs mois, même à 60°C, cela l’est davantage. Et d’autant plus, si cette mousse est élaborée par "chimie verte" à partir d’une substance naturelle. Enfin, cette mousse peut être rapidement détruite en modifiant simplement sa température, et ceci de façon réversible. C’est en résumé le travail réalisé par des équipes de l’INRA, du CEA et du CNRS, qui ouvre de nouvelles applications susceptibles d’intéresser les fabricants de cosmétiques ou de détergents. Les résultats de ces recherches sont publiés dans la revue Angewandte Chemie du 29 août.
|
Du fait de leur texture particulière et des molécules qui les constituent, les mousses ont souvent des vertus détergentes. En physico-chimie, les molécules, qu’il faut absolument disperser dans l’eau pour faire une mousse, sont dites "tensioactives". Elles se placent spontanément entre l’eau et l’air, ce qui permet de stabiliser des films d’eau très fins autour des bulles d’air de la mousse, selon une architecture particulière. De par leurs propriétés, les mousses ont de nombreuses applications dans des secteurs comme le nettoyage, la décontamination, la cosmétique, la lutte contre la pollution ou les incendies, l’agroalimentaire, ou l’extraction de ressources naturelles.
Les chercheurs de l’Inra, du CEA et du CNRS ont étudié ici une molécule tensioactive particulière, l’acide gras 12-hydroxy stéarique, issue de l’huile de ricin. Pour disperser cette molécule initialement insoluble dans l’eau, ils lui ont ajouté un sel. Ils ont ensuite démontré les propriétés très avantageuses de ce tensioactif : même en faible quantité, il produit une mousse abondante et, surtout, stable pendant plus de 6 mois, contrairement aux tensioactifs classiques qui ne stabilisent les mousses que quelques heures . Les chercheurs ont observé et expliqué ce phénomène par microscopie et diffusion de neutrons, permettant de suivre in situ l'évolution de la structure à l'échelle nanométrique.
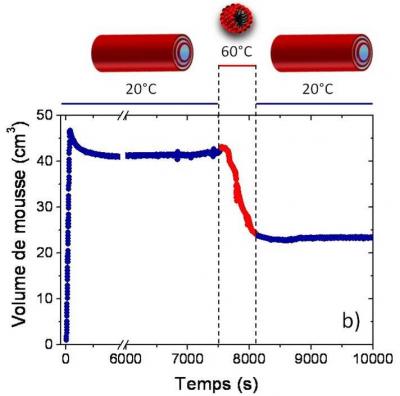
Evolution temporelle du volume de mousse, associée à une élévation temporaire de la température au delà du point critique.
Ainsi, ils ont montré que dans une gamme de températures moyennes, entre 20 et 60°C, l’acide gras 12-hydroxy stéarique, mélangé avec le "bon" sel, se disperse dans l’eau sous forme de tubes de quelques microns. Ces tubes forment alors une structure parfaitement stable et rigide dans les films d’eau très minces placés entre les bulles d’air, ce qui explique la tenue de la mousse.
Au-delà de 60°C, ces tubes fusionnent sous la forme d’assemblages sphériques mille fois plus petits (quelques nanomètres), que les chercheurs appellent des "micelles". La mousse auparavant stable s’effondre alors car la structure rigide disparait. Les chercheurs ont montré que cette transition d’un assemblage de tubes à un assemblage de micelles est « réversible ». En effet, si on augmente la température d’une mousse, son volume va diminuer dès la formation de micelles, et si on rabaisse la température entre 20 et 60°C, les tubes se reforment et la mousse se stabilise à nouveau (pour retrouver le volume de mousse initial, il faudrait tout de même réinjecter de l’air).
La constitution d’une mousse aussi stable avec une molécule tensioactive aussi simple et d’origine naturelle est une première. La température de transition entre l'état où la mousse contient des tubes, et l'état "micelles", dépend du sel choisi pour disperser la molécule dans l’eau, ce qui accroît son potentiel d’utilisation.
Cette chimie verte, puisqu’elle est issue d’une bio-molécule, ouvre des perspectives intéressantes car les mousses sont amplement utilisées dans l’industrie. Il serait par exemple possible de produire des détergents ou des shampoings dont on peut contrôler la quantité de mousse par simple effet de la température et ainsi en faciliter l’évacuation. Certains produits cosmétiques nécessitent de nombreux éléments chimiques afin d’obtenir une mousse stable ; l’utilisation de l’acide gras 12-hydroxy stéarique permettrait de limiter la quantité d’éléments synthétiques tout en conservant les propriétés "moussantes" plus longtemps.
Références :
|
Smart Foams: Switching Reversibly between Ultrastable and Unstable Foams, |
 |
 |
Communiqué de presse commun CEA, CNRS, INRA.
Contacts :
- Jean-Paul Douliez, Biopolymères Interactions Assemblages, INRA, Rue de la Géraudière, 44316 Nantes (France)
- Anne-Laure Fameau, Thèse cofinancée CEA-INRA.

• › Interfaces, fluides complexes et microfluidique
•  Institut Rayonnement Matière de Saclay • Laboratoire Léon Brillouin (LLB)
Institut Rayonnement Matière de Saclay • Laboratoire Léon Brillouin (LLB)
• Equipe "Diffusion petits angles"
• Diffractomètres de "diffusion de neutrons aux petits angles" : PACE, PA20, PAxy, TPA
